SU
Su; renksiz, kokusuz, saydam ve içerisinde çözünmüş kimyasal maddeler bulunduran bir sıvıdır. Yeryüzünde en yaygın olarak bulunan kimyasal bileşiktir. Kimyasal yapısı hidrojen ve oksijenden (H2O) ibarettir. Sıvı halde bulunan bileşiklerden mol ağırlığı en düşük olanıdır. Yoğunluğu saf haldeyken 1 g/cm³’tür.
İyi bir çözücü olduğundan bileşiminde daima çözünmüş kimyasal maddeler bulunur.
Doğadaki su bu nedenle hiçbir zaman saf olarak bulunmaz.
Saf su; mineraller, tuzlar ve diğer yabancı maddelerden tamamen temizlenmiş sudur ve ancak özel yöntemlerle elde edilir.
Suyun Molekül Yapısı
Su molekülü, dipol karakterdedir; çevresindeki elektrik yükü dağılımı üniform değildir. Su molekülünün oksijen tarafı elektronlardan zengindir ve lokal bir negatif (−) yüklü bölge oluşturur; hidrojen tarafı da elektronlardan fakirdir ve lokal bir pozitif (+) yüklü bölge oluşturur.
Su molekülleri, dipol karakterde oluşları nedeniyle hem katı halde hem de sıvı halde iken, birbirlerine hidrojen köprüsü bağlarla bağlanma yeteneğindedirler; bir su molekülünün bir hidrojen çekirdeği ile bir başka su molekülünün ortaklanmamış elektron çiftleri arasında, karşılıklı elektrostatik reaksiyonla bir hidrojen bağı oluşur:
Su moleküllerinin buzda %100’ü, oda sıcaklığındaki suda %70’i, 100oC’deki suda %50’si hidrojen bağlarıyla art arda birbirlerine bağlanmışlardır.
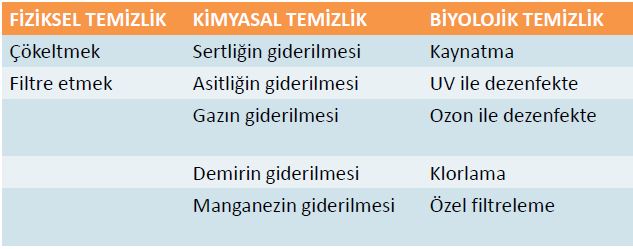
Su ve Buz
Suyun basit fakat çevre açısından son derece önemli bir özelliği de suyun sıvı hali üzerinde batmadan yüzebilen, suyun katı hali olan buzdur. Bu katı faz, (sadece düşük sıcaklıklarda oluşabilen) hidrojen bağları arasındaki geometriden dolayı, sıvı haldeki su kadar yoğun değildir. Hemen hemen tüm diğer maddeler için, katı form sıvı formdan daha yoğundur. Standart atmosferik basınçtaki taze su, en yoğun halini 3.98 °C'de alır ve daha fazla soğuması halinde yoğunluğu azalır.
Suyun donma sıcaklığı 760 mm Hg (1 atm) basınçta 0 C dir. Dondurulmuş su soğutma işleminde, bazı gıdaların üretiminde kullanılır.
Uygun tuzlar ile suyun donma sıcaklığı düşürülebilir. Örneğin 30 g Nacl ve 100 b buz karışımı -21 C de donar.
Çözücü Madde Olarak Su
- Bir molekül farklı atomlardan meydana gelmişse her bir atomun elektronlara karşı ilgisi farklı olur.
- Bunun sonucu olarak molekülün bir kısmında elektron fazlalığı ve bunun sonucu olarak da kısmi negatif yük, bir kısmında ise elektron noksanlığı ve bunun sonucu olarak da kısmi pozitif yük görülür.
- Bu şekildeki moleküllere polar moleküller denir.
- Su, bir polar moleküldür. Oksijen atomu bölgesi kısmen negatif, hidrojen atomları bölgesi ise kısmen pozitif yük gösterir.
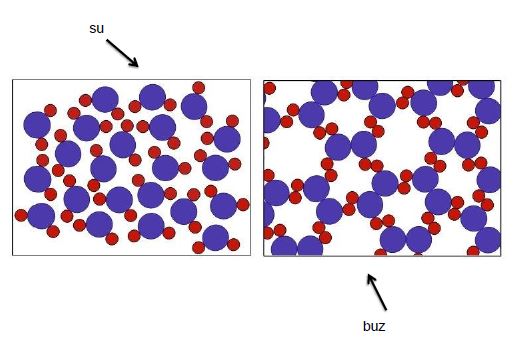
- Çözücünün su olduğu sistemlerde su molekülleri ile çevrilmiş pozitif veya negatif yüklü iyonlara hidrate iyon denir.
- Örneğin NaCl çözünmesinde, etrafı su molekülleri ile çevrilmiş olan Na+ ve Cl-iyonları birer hidrate iyondur.
- Pozitif veya negatif yüklüi yonların suda çözünmesi sırasında, etrafında yer alacak su moleküllerinin sayısı gelişi güzel olmayıp çoğunlukla önceden bellidir.

Suyun Sertliği
- Yüzey suları ve kaynak suları toprak tabakalrından çözünmüş olan değişik miktarlarda mineral içerir. Özellikle Ca ve Mg tuzları önemlidir. Bunlar suyun sertliğini olşturur.
- Sert su ile ellerin yıkanmasında el üzerinde sert ve kaba bir his oluşur.
- Et ve baklagiller sert suda zor pişerler.
- Sert su ile yapılan çay ve kahvenin tadı kötüleşir.
- Sert su ısıtma tesislerinde kazanlarda kireç taşlarını oluşturarak makineleri bozabilir.
- Sert sular serinleticidir.
- Suyun toplam sertliği karbonat sertliği ve karbonat olmayan sertlikten oluşur. Karbonat sertlik yapıcılar Ca ve Mg bikarbonatlardır. Nitrik, sülfürik, hidroklorik, fosforik ve salisik asitlerin Ca ve Mg tuzları ise karbonat olmayn setliği olşturur.
- Toplam sertlik(SB)=KS+KOS
- Suyun sertlik ölçüsü için Ca tuzları miktarı kullanılır. 1o sertlik 1 lt sudaki 1 mg CaO ve 2.4 mg CaSO4 veya 1.8 mg CaCO3 miktarına eşittir.

Gıdalarda Bulunan Su
 Serbest su:
Serbest su:
gıda içinde solvent ya da çözücü olarak buluna sudur. Gıdada bulunan çeşitli besin elementleri suda erimiş olarak bulunur. Gıdadaki çeşitli bozulmalar serbest su ile ilgilidir. Gıdada fiziksel değişimler meydana getirir.
Adsorbe su:
gıdada yarı bağlı veya tabaka halinde bulunan sudur. Gıda bileşenlerin Veya yapısal moleküllerin yüzeyine ince bir film halinde bağlanmıştır. Toplam suyun yaklaşık %10-15 ini oluşturur.
Bağlı su:
gıda bileşenlerin yapısına girmiş veya bunlara tek bir molekül tabakası halinde H bağlaı ile bağlanmış su formudur. Protein, karbonhidrat, asit ve tuzlara bağlı olan sudur. Bu suya hidratize su, hidrasyon suyu, kristal su veya kimyasal su isimleri de verilir. Gıdada %3-5 oranındadır. -40 oC de donmayan sudur.
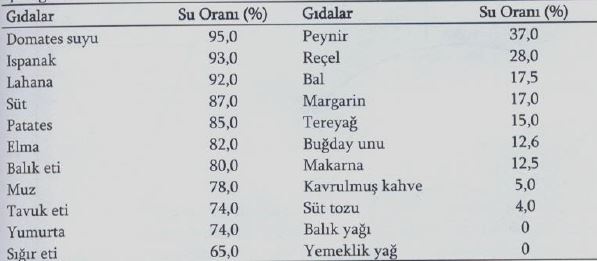
Gıdalarda bulunan su miktarı önemli bir kalite göstergesidir. Çünkü bazı gıdalarda su oranı yüksek olursa hem kalite özellikleri değişir hem de enzim ve mikroorganizmalar tarafından kısa sürede bozulmaya neden olur.
Gıdaların içerdiği su birçok bileşen için çözücü görevi görür. Gıdalardaki biyolojik ve kimyasal değişikliklerden kaynaklanan bozulmaların sebebi gıdaların yüksek miktarda su içermesidir. Bu nedenle su miktarının düşürülmesi için pek çok gıda muhafaza yöntemi geliştirilmiştir. Kurutma ve konsantre etme gibi yöntemler gıdadaki su miktarını azaltmayı ve böylece çözünenlerin miktarını artırmayı amaçlamaktadır. Bu yöntemler, çözücünün fiziksel özelliklerini değiştirir.
Gıdalardan suyun ayrılması ve gıdaya çözünen madde eklenmesi aynı gibi görünse de gıda üzerindeki etkileri farklıdır. Örneğin gıdanın içeriği çözelti, mikrobiyolojik gelişmenin kontrol edilebildiği noktaya kadar konsantre edildiğinde istenmeyen fiziksel ve kimyasal değişiklikler ortaya çıkabilir. Konsantrasyonun çok büyük miktarda artırılması, enzimatik ve enzimatik olmayan değişmeleri önlemek için gerekebilir. Bu taktirde de gıdanın tadında ve görünüşünde değişmeler gözlenir.
Gıdalarda su miktarını % nem olarak ifade ederiz ve gıdalarda nem miktarının kontrol edilmesinin nedenlerini şu şekilde ifade edebiliriz:
- Depolama açısından nem miktarı önemlidir. Çünkü gıdadaki enzim ve mikroorganizma faaliyetleri nem miktarına bağlıdır. Nem miktarı arttıkça enzim ve mikroorganizma faaliyetleri de artar ve gıda bozulmaya başlar.Depolama kriterlerinin belirlenmesinde gıdanın nem miktarına da bakılır.
- Ticari açıdan önemlidir. Örneğin fire kayıpları ve fiyatın düşük olması gibi.
- Standartlardaki nem oranını karşılaştırmak açısından önemlidir. Analiz sonuçlarının belli bir nem sınırı üzerinden verilmesi gibi.
- Gıdalara uygulanacak işlemlerin
Su Aktivitesi
Suyun besin maddesindeki durumu; besinin su içeriği ve bulunduğu ortamın bağıl nemliliği arasındaki ilişki yardımıyla tanımlanır ve buna su aktivitesi denir.
aw = P1 / P0 x 100 Su aktivitesine göre gıdalar - 0.9-0.999: yüksek nemli gıdalar
>%50 su
Taze et, meyve, sebze, peynir
- 0.6-0.9: orta nemli gıdalar
%10-50 su
Reçel, bazı peynirler, kurutulmuş meyveler, kek
- <0.6: düşük nemli gıdalar
Tahıllar, yemişler, kurutulmuş gıdalar
Mikroorganizmalar susuz yaşayamazlar ve Her mikroorganizma için optimum aw değeri vardır.
aw düşük olduğunda mikrobiyal gelişme gecikir.
- <0.60 mikrobiyal gelişim olmaz
- 0.60-0.85 maya, küf, ozmotik basınca dayanıklı bakteriler
- <0.85 patojenler gelişemez
- 0.87-0.90 maya ve küfler gelişebilir
- 0.91-0.95 bozulma yapan bakteriler, bazı küfler
- >0.95 patojen ve bozulma yapan bakteriler, bazı mayalar
Gıdanın bozulmasında ilk reaksiyon yağların acılaşmasıdır ve 0-0.2 su aktivitesi değerinde oldukça yaygındır.
İkinci reaksiyonlar Maillard reaksiyonlarıdır ve enzimatik olmayan esmerleşme reaksiyonları olarak önemlidir. Bu olaylar 0.6-0.7 su aktivitesi değerlerinde maksimum hıza ulaşır.
Depolama ve ambalajlamada su aktivitesi önemlidir.
Gıda Üretimi İçin Hammadde Olarak İçme Suyu
- İçme suyu hiçbir patojen mikroorgarnizma içermemelidir.
- Toksik maddelerden arınmış olmalıdır.
- Berrak ve serin olmalı, hoş bir tat göstermelidir.
- Renksiz ve kokusuz olmalıdır.
- Belirli bir sertlik derecesinde olmalıdır.
Su temizleme yöntemleri