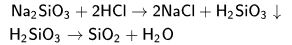SİLİS
a. (fr. silice). Miner. Pek çok mineralde bulunan, Sİ02 formülünde oksijenli silisyum bileşiği.
—Camc.
Silis camı, erimiş kuvarstan elde edilen cam. (Silis camı, yaygın olarak kullanılan cisimler içinde en küçük genleşme katsayısına sahip cisimdir ve morötesi ışınlara karşı yüksek bir geçirgenlik gösterir.)
—Pedol.
Silis ayrılması, toprakların ve yüzeysel kayaçların içerdiği silikatlı minerallerin bozunarak silisi bırakmasıyla sonuçlanan jeokimyasal evrim.
—Teknol.
Silis giderme, sınai sularda bulunabilecek silisi gidermek için yapılan işlem.
—ANSİKL. Bot
. Silis bitkiler tarafından ancak koloidal biçimde özümlenebilir ve bu bakımdan bazı topraklar (çeltik tarlaları) geçici olarak bu elementten yoksun kalabilir. Bitkilerin çoğunda ender bulunan silis, bazı türlerde (çayırsazı, atkuyruğu, buğdaygiller), özellikle üst deri hücrelerinde bol miktarda yer alır ve bu bitkileri sert, pürüzlü, hatta kenarlarını keskin kılar. Diyatomelerin silisli kılıflarının kalıntıları zımpara gibi kullanılır.
—Eczc. Koloidal silis ilaç yapımında, nem çekici olarak birçok preparatın bileşimine girer ve emülsiyonlara jel özelliği vermek için kullanılır. Potasyum ve sodyum silikat, ortopedide, alçıların sertleştirilmesinde kullanılır.
—Kim. Laboratuvarlarda, amorf ya da kristalleşmiş doğal silis biçimlerinden baş- ,ka iki çeşit yapay amorf silis kullanılır; bunlardan ilki silis camı, İkincisi silis peltesidir.
1. Silis camı, cam görünüşünde saydam bir maddedir; kuvarsın ergitilmesi ve ergitme sonunda oluşan ağdalı sıvının yeniden soğutulmasıyla elde edilir. Isıl genleşme katsayısının son derece küçük olması, kimyasal etkenlere karşı iyi bir direnç göstermesi, yalıtıcı özellikler taşıması ve morötesi ışınlara karşı yüksek geçirgenlik göstermesi nedeniyle laboratuvar aygıtları ile cıva buharlı ampul yapımında cama tercih edilir
2. Silis peltesi, bileşiminde yaklaşık % 4 oranında su bulunan yarısaydam ve granüllü bir maddedir. Bir alkali metal silikat çözeltisinin asilleştirilmesi ve tepkime sonunda oluşan tıkız peltenin suyunun giderilmesiyle elde edilir. Silis jelinin geniş bir özgül yüzeyi vardır; bu nedenle kurutma etkeni, katalizör taşıyıcısı (S02'nin S03'e yükseltgenmesinde V205 taşıyıcısı) ya da doğrudan katalizör olarak (arilli halojenürlerin fenollere hidrolizi) işe yarar. Petrolün krakinginde alümin ve silisten oluşan karma bir pelte kullanılır. Silis peltesinin yüzde tutma özelliklerinden ayrıca kromatografi çözümlemelerinde yararlanılır. Silis, kimyasal bakımdan son derece kararlı bir maddedir; ısı etkisiyle ayrışmaz, indirgenmesi çok zordur. Elektrik fırınında karbonla ayrışarak karbonmonoksit (CO) ile silisyum karbürü (SiC) verir. Alkali metaller ya da magnezyum, silisi indirgeyerek silisyumun ayrılmasını sağlar.
Silis bir asit anhidrittir; yüksek sıcaklıkta metal oksitlerle bileşerek tek başlarına elde edilemeyen kararsız silikatları verir; bunlar ortosilisik asit (HSiO, metasilisik asit (HSiC) ve yoğuşmuş polisilisik asitler (2, 3 vb.) gibi silisyum atomu taşımalarına bağlı olarak disilisik, trisilisik denen asitler) gibi çeşitli silisik asitlerin tuzlarıdır. Bu silikatlar ayrıca silisin karbonatlar ya da sülfatlar üzerine etkimesi sonunda da elde edilebilir (cam üretimi).
Silis, hidrofluorik asit dışında hiçbir asitten etkilenmez; hidrofluorik asitle tepkimeye girdiğinde silisyum flüorür gazına (SiFJ dönüşür.
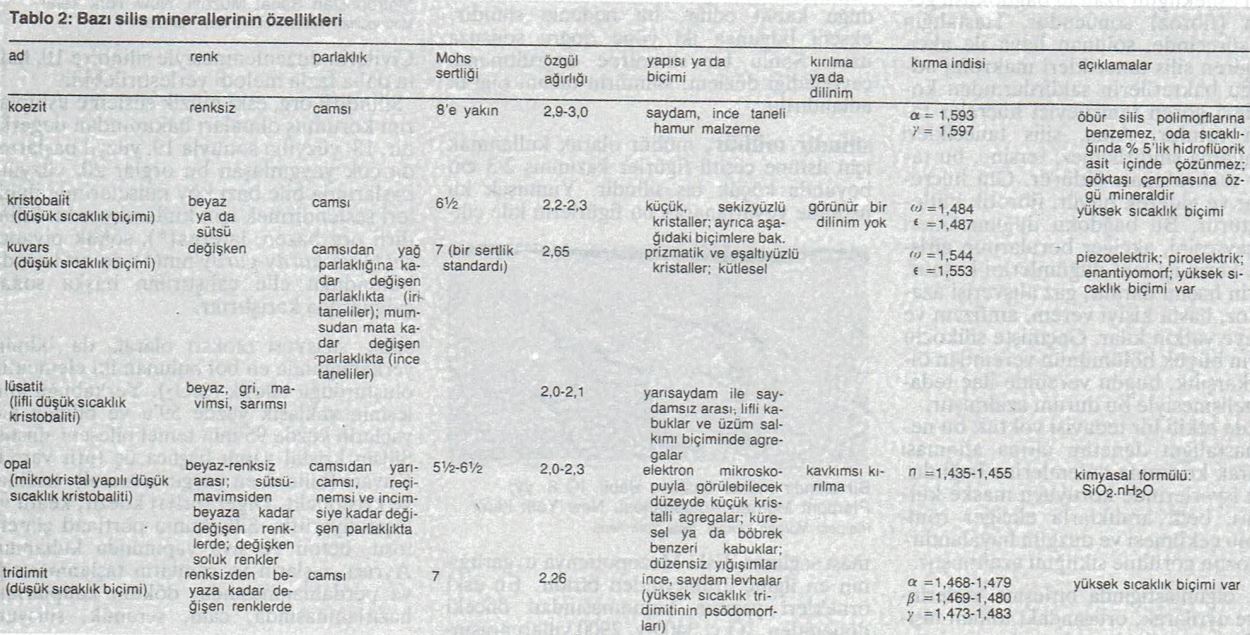
—Miner. Silis ailesi, genellikle saf olmayan Sİ02 oksidinin oluşturduğu bütün mineral türlerini ve çeşitlerini kapsar (kuvars, kalseduan, çakmaktaşı, opal, tridimit vb.)
—Tip. Silis tozlarının solunum yoluyla alınması silikoza neden olur.
Kaynak: Büyük Larousse
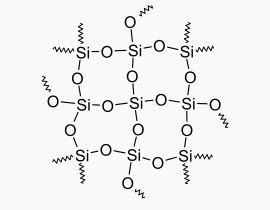

 Bileşikler - Silisyum dioksit
Bileşikler - Silisyum dioksit