Ziyaretçi
metal bağı,
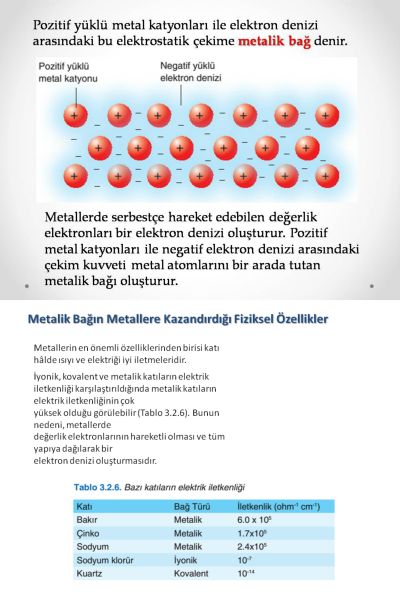
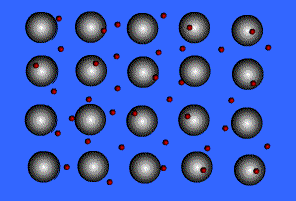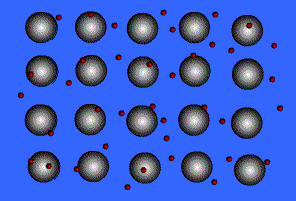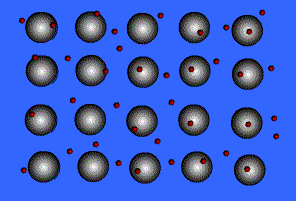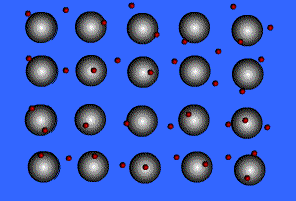
bir metalin atomlarını bir arada tutan kuvvet. Metallerdeki atomlar yakın birleşmiş bir biçimde düzenlenmiştir ve metallerin çoğunda atomların her birinin en dış elektron kabuğu çok sayıda komşu atomun üstüne biner. Bunun sonucunda değerlik (valans) elektronları sürekli olarak bir atomdan öbürüne hareket eder ve belirli bir atom çiftinin üzerinde bulunmaz. Yani metallerdeki değerlik elektronları, ortaklaşım (kovalans) bağlı maddelerdekilerin tersine yerleşik değildir ve tüm kristalin içinde oldukça serbest biçimde gezinir. Elektronları uzaklaşan atomlar artı yüklü iyonlar haline geçer ve bu iyonlar ile değerlik elektronları arasındaki etkileşim metal kristalini bir arada tutan çekimi ya da bağlanma kuvvetini oluşturur.
Sponsorlu Bağlantılar
Metallere özgü özelliklerin çoğu değerlik elektronlarının yerleşik olmamasına ya da serbest olarak hareket etmelerine bağlanır. Örneğin metallerin elektrik iletkenliklerinin yüksek olmasının nedeni elektronların bu davranışıdır. Isıl bir etki olmadan metale bir elektrik alanı uygulandığında değerlik elektronları ortaklaşım bağlı kristallerde olduğu gibi atomlardan uzaklaşabilir. Metal iyonları arasındaki bağ kuvvetinin yönü olmamasının yanı sıra hareketli değerlik elektronlarının bulunması da çoğu metale dövülgenlik ve süneklik özelliği kazandırır. Bir metale biçim verildiğinde ya da metal çekildiğinde malzeme kırılmaz, çünkü kristal yapısındaki düzlemlerde bulunan iyonlar birbirlerine göre oldukça kolay yer değiştirebilir. Ayrıca yerleşik olmayan değerlik elektronları, yüklü iyonlar arasında bir tampon görevi görür ve bu iyonların bir araya gelmesini ve kristalin kırılmasına yol açacak güçlü itme kuvvetlerinin oluşmasını önler.
kaynak: Ana Britannica
BAKINIZ Kimyasal Bağlar ve Hibritleşme
Son düzenleyen Safi; 22 Kasım 2016 04:42

 Metalik Bağı
Metalik Bağı