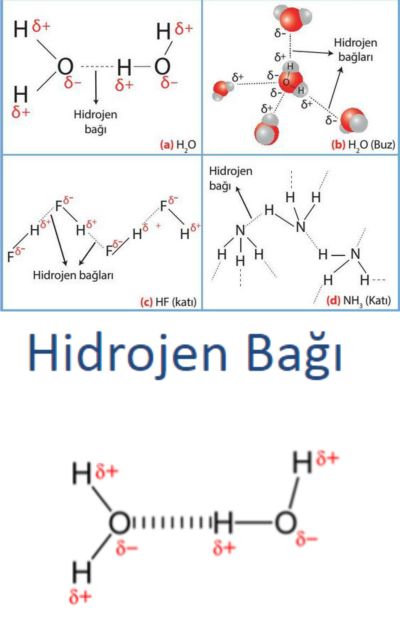
Hidrojen Bağı (Hydrogen Bonding)!
Hidrojen bağı, özellikle
buzda olmak üzere birkaç kristalde önemlidir. Elektron ile bir hidrojen atomu genellikle bir
elektronegatif atom ile tek bir kovalent bağ oluşturur. Hidrojen bağında atom bir protona iyonlaştırılır. Proton iki anyon arasında oturur ve onları birleştirir.
Hidrojen bağı sadece
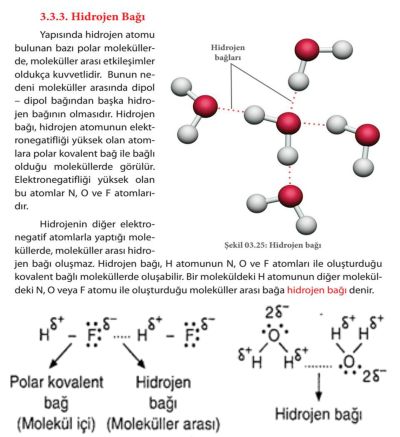
en yüksek elektronegatif iyonlarla oluşur:
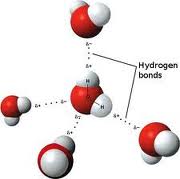
Azot, Oksijen ve Flor. Suda hidrojen, oksijen iyonlarının çiftlerini bağlar. Su, birçok farklı kristal yapısında bulunur, ancak bunların hepsi, hidrojen atomlarının oksijen çiftleri arasında oturması özelliğine sahiptir. Bir başka hidrojenle bağlanmış katı,
hidrojen atomunun (proton) flor çiftlerini bağladığı hidrojen florürdür (HF). 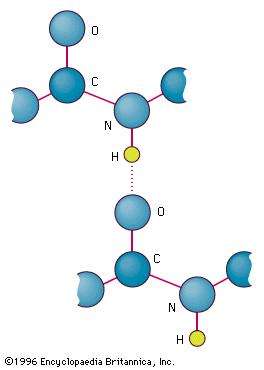 Peptit Bağlarında Hidrojen Bağı!
Peptit Bağlarında Hidrojen Bağı! olarak tanımlanabilir. Böyle bir bağ, bir iyonik bağ veya kovalent bağdan daha zayıf, ancak
van der Waals kuvvetlerinden daha güçlüdür. Hidrojen bağları, farklı moleküllerdeki veya aynı molekülün parçalarındaki atomlar arasında bulunabilir. Çiftin bir atomu
(donör), genellikle bir flor, nitrojen veya oksijen atomu, elektronları eşit olmayan şekilde paylaşan bir hidrojen atomuna
(−FH, −NH veya −OH) kovalent olarak bağlanır; yüksek elektron afinitesi Hidrojenin hafif bir yüke maruz kalmasına neden olur.
Paritenin diğer atomu da, tipik olarak
F, N veya O, hafif bir negatif yük veren, birleşik olmayan elektron çiftine sahiptir. Esas olarak
elektrostatik çekim yoluyla, verici atom, hidrojenini alıcı atomla etkin bir şekilde paylaşır ve bir bağ oluşturur. Geniş hidrojen bağı nedeniyle su (H2O), büyüklüğünde bir molekül için beklenebilecek çok daha yüksek sıcaklıklarda sıvıdır.
Su aynı zamanda iyonik bileşikler ve diğer birçokları için iyi bir çözücüdür çünkü çözünen ile hidrojen bağlarını kolayca oluşturur. Bir doğrusal protein molekülündeki amino asitler arasındaki hidrojen bağı,
fonksiyonel konfigürasyona katlanma biçimini belirler. Azotlu bazlar arasında hidrojen bağları nükleotid iki şerit üzerinde
DNA (Guanin ile çiftler Sitozin, Adenin ile Timin) iletilmesi için çok önemlidir
(Çifte sarmal yol genetik bilgi). Kaynak: AnaBritannica


 Hidrojen Bağı
Hidrojen Bağı