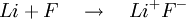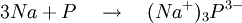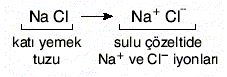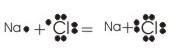Ziyaretçi
iyon bağı
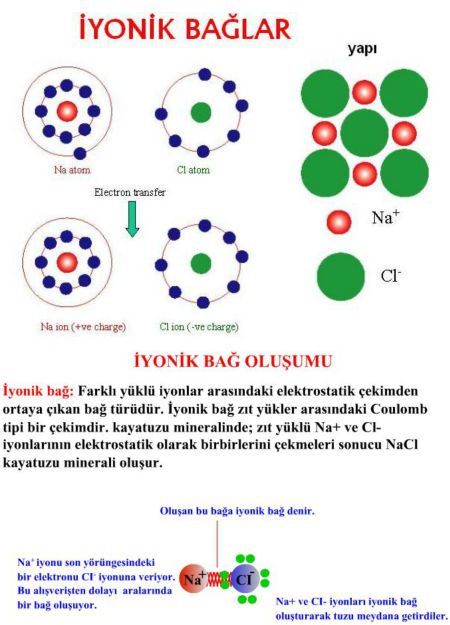
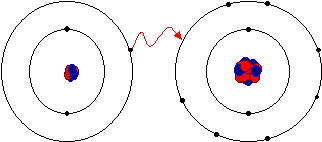
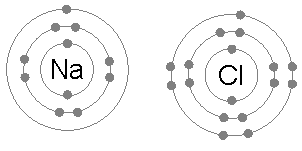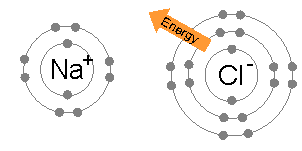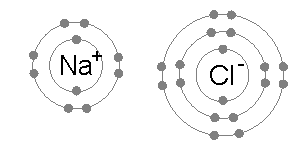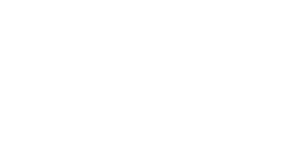
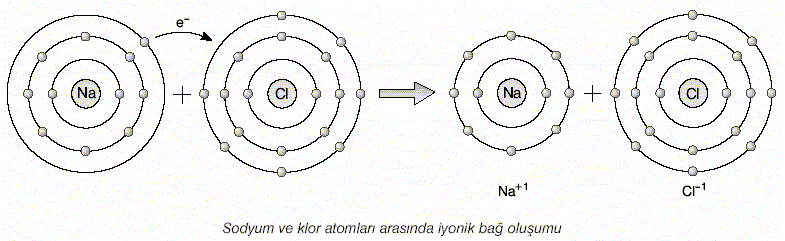
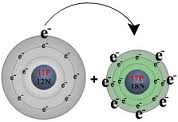
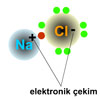
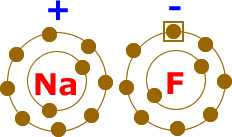
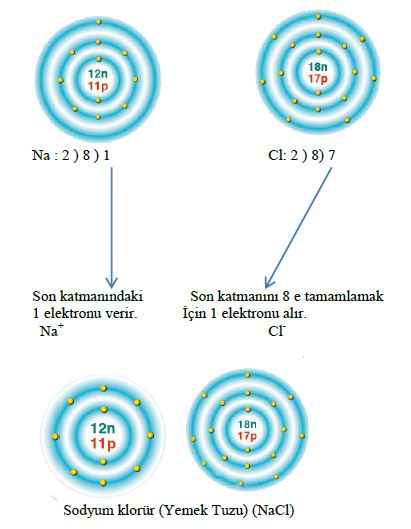
ELEKTROVALANS BAĞİ olarak da bilinir, bir kimyasal bileşiğin karşıt elektrik yüklü atomları arasında oluşan bağ. Bu tür bağ bir atomun en dış yörüngemsisindeki değerlik (valans) elektronlarının kalıcı biçimde bir başka atoma geçmesi durumunda oluşur. Elektronlarını kaybeden atom artı elektrik yüklü iyon (katyon), elektron kazanan ise eksi elektrik yüklü iyon (anyon) haline geçer. 19. yüzyılın sonlarında atomlar arasında elektron aktarımı konusuna ilişkin olarak İngiliz fizikçi J. J. Thomson’ un geliştirdiği düşünceyi 1916’da Alman bilim adamı Walter Kossel iyon bağı kuramı durumuna getirdi.
Sponsorlu Bağlantılar
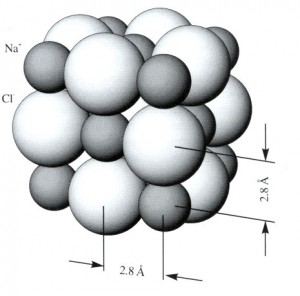
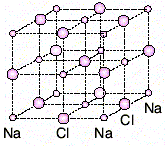
Atomların iyon bağıyla bağlanması sonucunda iyon ya da elektrovalans bileşikleri oluşur; bunların en iyi bilinen örnekleri alkali ve toprak alkali metallerin hidrürleridir. İyon bağıyla bağlanmış kristalin katilarda, karşıt elektrik yüklü parçacıklar arasındaki elektrostatik çekim kuvvetleri ve benzer elektrik yüklü parçacıklar arasındaki elektrostatik itme kuvvetleri nedeniyle iyonlar, her artı yüklü iyon, eksi yüklü iyonlarla ve her eksi yüklü iyon, artı yüklü iyonlarla sarılacak biçimde düzenlenir. Eksi ve artı yüklü iyonlar, birbiri ardına gelecek biçimde düzenlendiğinden yükler birbirini dengeler ve cisim elektriksel bakımdan nötr olur. İyon bağıyla bağlanmış kristallerdeki elektrostatik kuvvetler oldukça etkili olduğundan bu yapıdaki cisimler serttir ve uçucu değildir. Ama iyon bağları dielektrik sabiti yüksek olan ortamlarda önemli ölçüde zayıflar.
İyon bağıyla bağlanmış bileşiklerin, aynı zamanda ortaklaşım (kovalans) bağları içerdiği kabul edilir; iki, ender olarak da üç atom arasında, atomlardan her birinin değerlik elektronlarından birini öteki atomla paylaşması sonucunda ortaya çıkan ortaklaşım bağında, iyon bağında olduğu gibi kalıcı elektron aktarımı olmaz.
kaynak: Ana Britannica
Son düzenleyen Safi; 22 Kasım 2016 20:31

 İyonik Bağ
İyonik Bağ