Ziyaretçi
Arama
 İnsan vücudundaki tampon görevi gören çözeltiler nelerdir?
İnsan vücudundaki tampon görevi gören çözeltiler nelerdir?
Güncelleme: 3 Ocak 2017 Gösterim: 25.066 Cevap: 2
Ziyaretçi
17 Mart 2010
Mesaj #1
Bu mesaj 'en iyi cevap' seçilmiştir.
Sponsorlu Bağlantılar
BAKINIZ
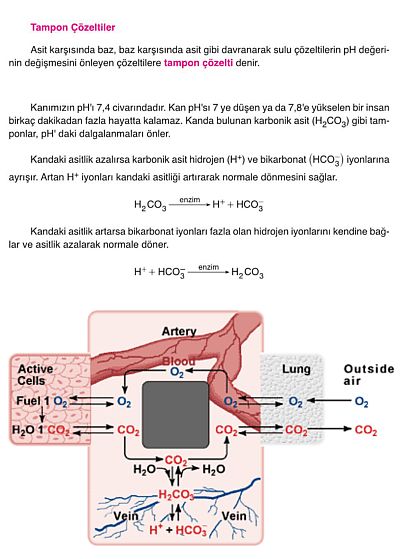
Tampon Çözeltiler
Kan Nedir - Kanın Yapısı, Özellikleri ve Görevleri
SİLENTİUM EST AURUM
Asit Baz Dengesi
Homeostasisin (vücudun iç dengesi) sağlanması için sıvı ve elektrolit dengesinin sağlanması yanında asit baz dengesinin sağlanması da oldukça önemlidir. Vücut sıvılarındaki hidrojen iyonu (H+) konsantrasyonunun düzenlenmesine asit baz dengesi denir. Vücut sıvılarında çok az miktarda H+ iyonu bulunmasına rağmen H+ iyonu konsantrasyonundaki çok küçük değişiklikler bile enzimatik reaksiyonları ve fizyolojik olayları etkiler.
Sağlıklı bir yaşam için organizmanın asit miktarının yani H+ iyonlarının dengede tutulması gerekir. Bir eriyiğin asitlik derecesi o eriyiğin içindeki H+ iyonu miktarı ile ölçülür. Solüsyonların H+ iyonu yoğunlukları “pH” ile ifade edilir. Buradaki “p” (power) güç anlamına gelir. “H” ise hidrojen iyonudur.
Suda çözündüklerinde H+ iyonu veren maddelere asit denir. Suda çözündüklerinde OH" (hidroksil) taşıyarak H+ iyonu alan maddelere ise baz adı verilir. Total pH ölçeği 0 ile 14 arasında değişir. Asit ve baz değerlerinin toplamı 14’tür.
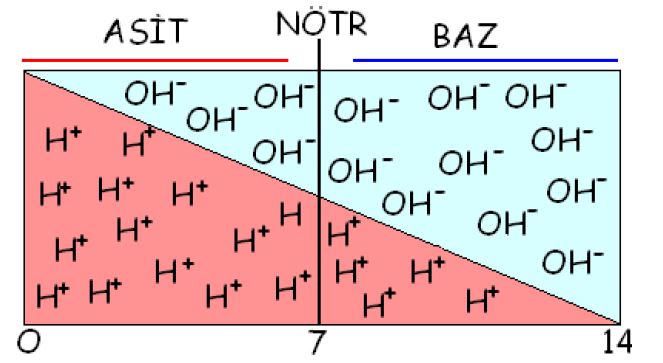
Suyun pH’ı 7 yani nötrdür. pH’ ı 7’den küçük alan eriyikler asit, pH’ ı 7’den büyük olan eriyikler ise baz yani alkalendir. Vücut sıvılarının pH’ı hafif alkalidir.
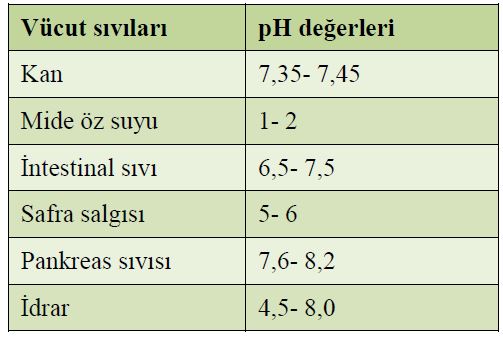
Kanın pH’ı ortalama olarak 7,40 olarak kabul edilir. Arteriyel kanın (atardamarlardaki temiz kan) pH’ı 7,45 venöz kanın (toplardamarlardaki kirli kan) ise 7,35’tir. Bazı vücut sıvılarının pH’ı tablo 1.2’de verilmiştir.
Kan pH’ın; 6,9 (asidoz) veya 7,8 (alkaloz) olması ağır hastalık tablolarını gösterir.
- Asidoz: Ekstrasellüler sıvıda H+ iyonu konsantrasyonunun artması yani pH değerinin düşmesi hâlinde ortaya çıkan tablodur.
- Alkaloz: Ekstrasellüler sıvıda H+ iyonu konsantrasyonunun azalması yani pH değerinin yükselmesi hâlinde ortaya çıkan tablodur.

Asit Baz Dengesini Sağlayan Sistemler
Hücre metabolizması sonucunda vücutta bazı atık maddeler ve asitler açığa çıkarak kan pH değerinde değişikliklere neden olur. Vücutta bu asitlerin nötralize edilerek ve atılarak pH değerinin dengede tutulması birtakım kimyasal tampon sistemleri, akciğerler ve böbrekler tarafından sağlanır.
Vücut Sıvılarının Kimyasal Asit Baz Tampon Sistemleri
Vücut sıvılarında bulunan kimyasal tampon sistemleri, H+ iyonu konsantrasyonunda bir değişiklik meydana geldiğinde kısa sürede reaksiyona girer. Bu tampon sistemler, H+ iyonlarının vücuttan atılmasını engelleyerek vücut sıvılarında fazla bulunan asit ve alkali maddelerle birleşir. Böylece bu maddeleri kendilerine bağlı tutarak meydana gelen dengesizliği düzeltmeye çalışır.
Bu tampon sistemler:
Bikarbonat tampon sistemi
Genel olarak ekstrasellüler sıvıların tampon sistemidir. Bu tampon sistemi ile hücre dışı sıvıdaki H + iyonlarının % 90’ını kontrol altında tutar. Bikarbonat tampon sistemini zayıf bir asit olan karbonik asit (H2CO3) ile sodyum bikarbonat (NaHCO3) oluşturur. Karbonik asit (H2CO3) vücutta karbondioksitin su (H2O) ile reaksiyonu sonucunda meydana gelir.
Fosfat tampon sistemi
Daha çok intrasellüler sıvıların tampon sistemidir. Eritrositlerde ve böbrek tubulus hücrelerinde daha çok görev alır. Fosfat tampon sistemleri, böbreklerden H+ iyonlarının atılmasında önemli rol oynar.
Proteinler hücre içinde çok fazla bulunduklarından tampon olarak önemli role sahiptir. Doku hücrelerinde, intrasellüler sıvıların önde gelen tampon sistemlerindendir. Protein tampon sistemi hem bazik hem de asidik tamponlama işlevi görür.
DEVAMI Kan Nedir - Kanın Yapısı, Özellikleri ve Görevleri
SİLENTİUM EST AURUM
Benzer Konular
| 3 Mart 2010 / Misafir Soru-Cevap |
| 3 Ocak 2017 / kompetankedi Kimya |
| 27 Nisan 2013 / Misafir Soru-Cevap |
| 3 Temmuz 2011 / And Soru-Cevap |
| Kapat Saat: 03:40 Hoş Geldiniz Ziyaretçi
Benzer Konular
Son MesajlarYenile Yükleniyor... |


