Ziyaretçi
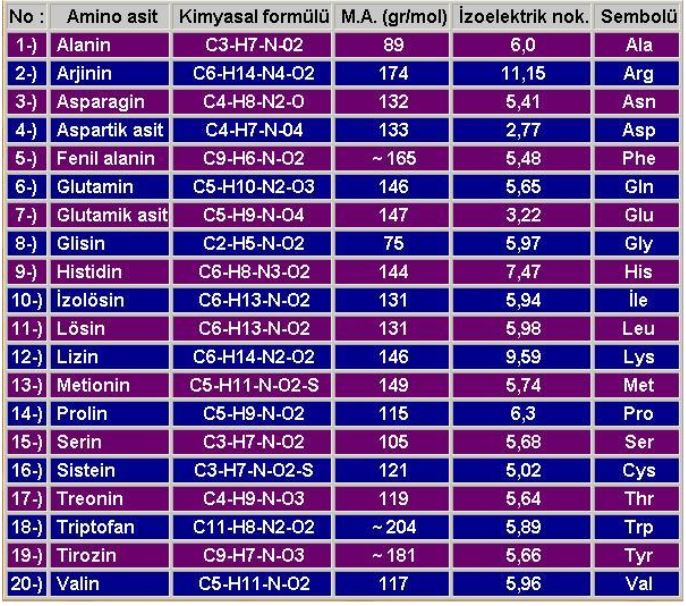
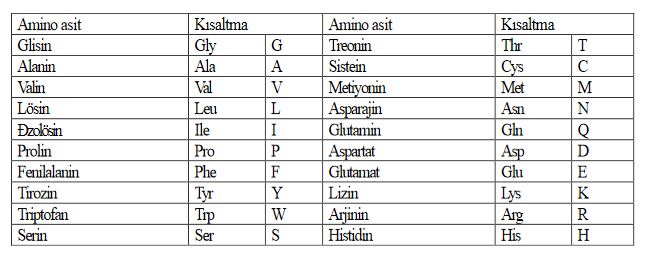
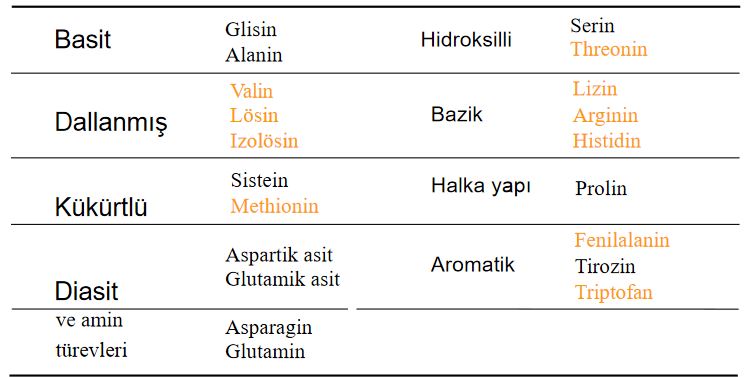
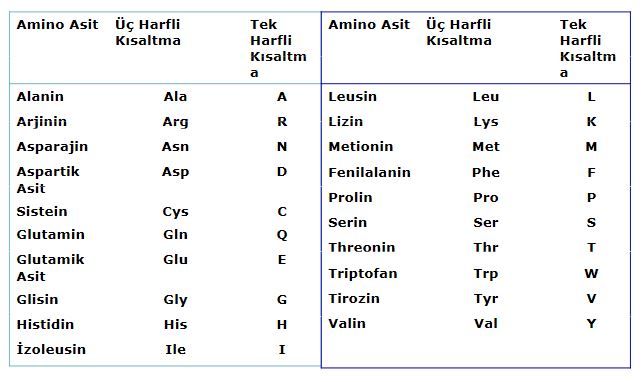
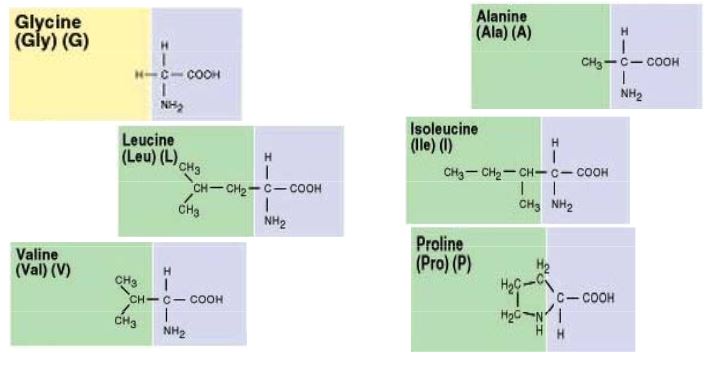
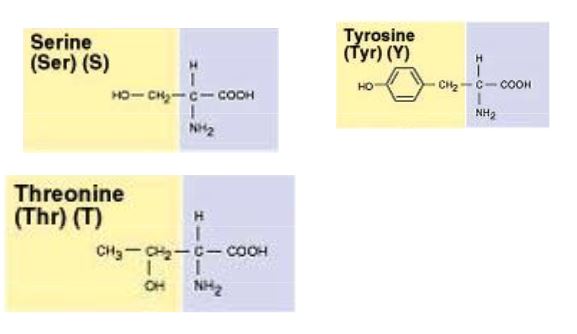
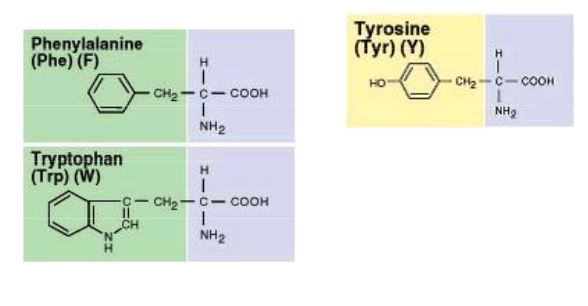
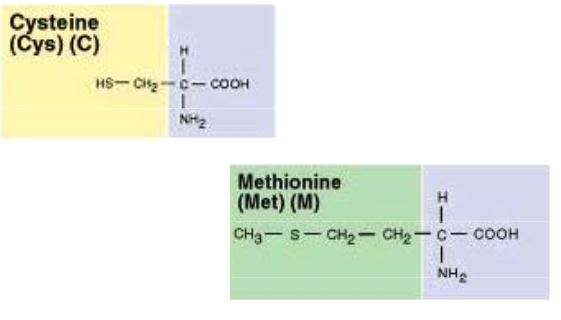
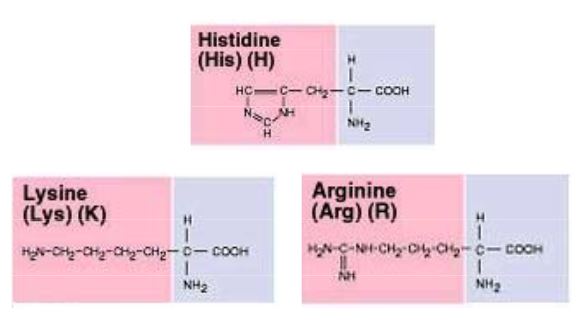
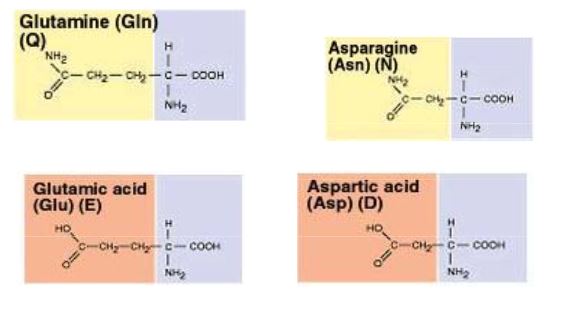
Amino asitler
Bir ya da birden çok amino grubu içeren karboksilli asitler.
Sponsorlu Bağlantılar
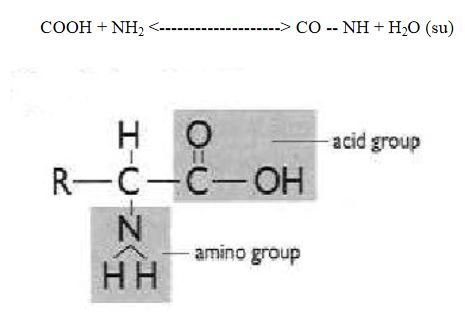
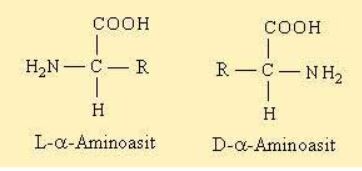
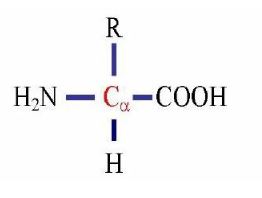
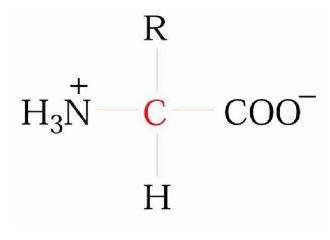
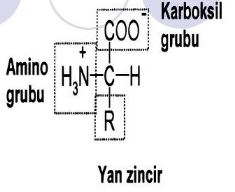
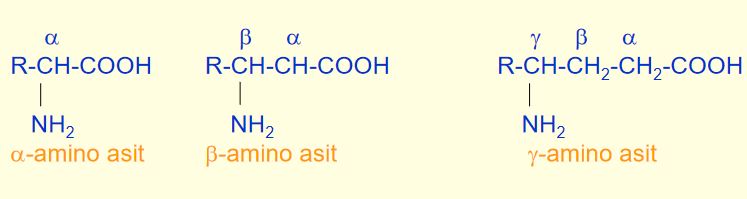
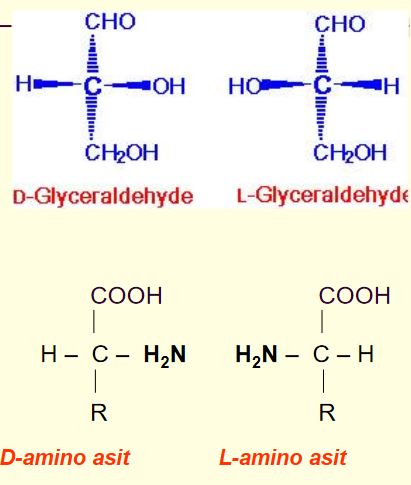
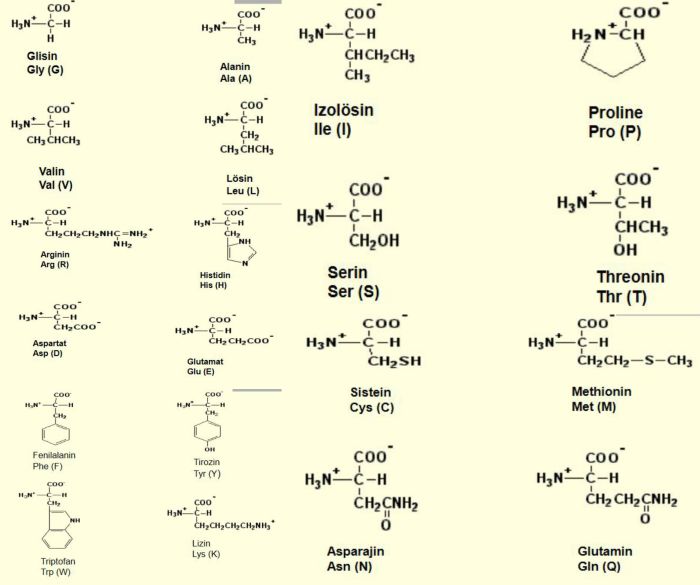
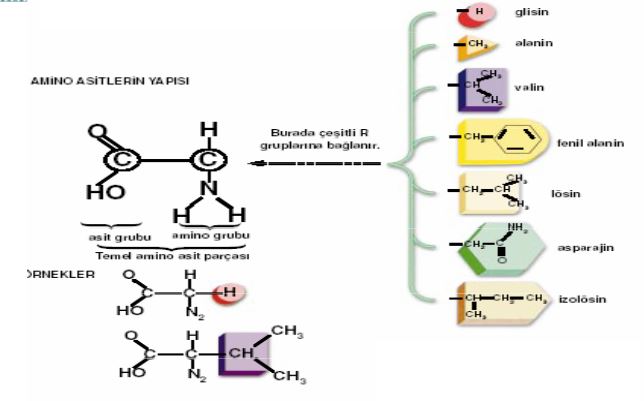
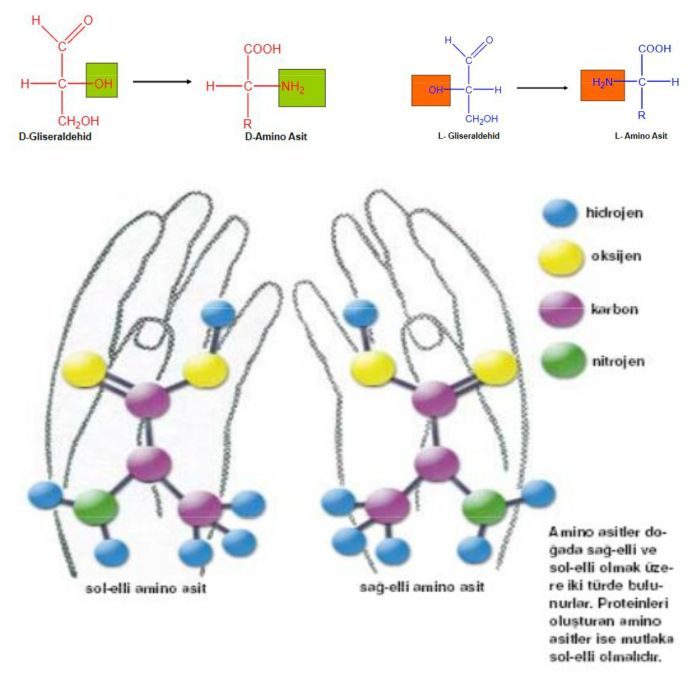
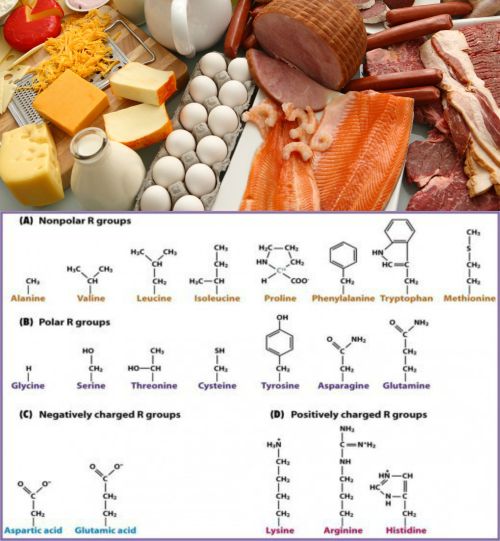
Birçoğunun özel adları olmakla birlikte, aminoasitler, amino grubunun yeri, karboksilden sonra gelen karbon atomları, alfa, beta, gamma harfleriyle belirlenerek, türedikleri karboksilli asidin adıyla adlandırılırlar (alfa amino propiyonik asit). Aminoasitler beyaz, kristal yapılı, suda çözünen, amfoter katılardır. Alkol ve eterde çözünmezler. Uçucu değildirler. Bütün canlılarda bulunan proteinlerin yapıtaşlarını yirmi dolayında alfa amino asiti oluşturur. (RCH [NH2] COOH) genel formülüyle gösterilen alfa aminoasitler (glisin dışında), karboksil grubunun (COOH), amino grubunun (NH2), hidrojen atomunun ve ilgili aminoasidin niteliğini belirleyen özgün bir grubun bağlandığı asimetrik bir karbon atomu içerirler; öyle ki aminoasitler birbirinin ayna olan iki ayrı biçimde olabilirler.
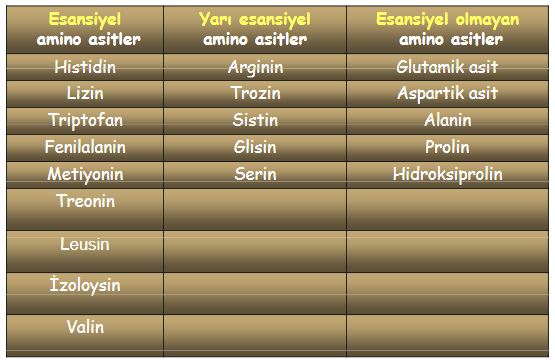
Her aminoasitte bir asit ve bir amino grubu bulunduğu için, aminoasitler, amit bağları aracılığıyla peptit denen uzun bir aminoasit zinciri oluşturabilirler. Peptit sentezi, protein sentezinin bir aşamasıdır. Böylece aminoasitler, hormonlara, enzimlere ve nükleik asitlere dönüşürler. Örneğin tirosin aminoasidi, tiroid bezince salgılanan tiroksine, ayrıca cilde renk veren boya maddesini oluşturan melanine dönüşür. Histidin aminoasidi, yaralı dokularca salgılanan ve vücudu koruyucu etki gösteren histamine dönüşür. Proteinler de, sindirim sırasında olduğu gibi, hidroliz yoluyla, kendilerini oluşturan aminoasitlere parçalanabilirler. Aminoasitlerden amino grubu çıkınca, azot, üre olarak idrarla vücuttan atılırken, molekülün geri kalanı, sitrik asit çevrimine girerek parçalanır ve enerji sağlar. Besin maddeleriyle vücuda giremeyen bazı aminoasitlerse, vücut içinde üretilirler. Yaşam için vazgeçilmez olup ancak besinlerden sağlanabilen sekiz doğal aminoasit vardır. Aminoasitlerin yapay sentezleri için daha çok asit türevlerinin amonyak ya da türevlerine etkisinden yararlanılır. Stenley Miller yöntemiyle, 20 kadar aminoasit sentezi gerçekleştirilebilmektedir. Bu yöntemi; hidrojen, metan gazı, su buharı ve amonyağın, serbest oksijensiz bir ortamda birkaç gün yüksek elektriksel deşarjda kalmasına dayanır. Birçok biyokimyacı, ilk canlı moleküllerin böyle oluştuğunu sanmaktadır. Besinlerin kan aracılığıyla vücuda dağıtılması nedeniyle kanda daima serbest aminoasitler bulunur. Normal olarak insan kanının bir litresinde 200 miligram aminoasit vardır. Canlı organizmaların evrimini, kanlarındaki aminoasit grupları sayısından hareketle açıklamaya çalışanlar da vardır. Kandaki aminoasit miktarının saptanması, bazı hastalıkların teşhisini de sağlar. Bu analizlere aminoasidemi denir. Aminoasidüriyse, idrardaki aminoasit miktarının fazlalığı demektir ve karaciğer yetmezliğinin belirtisidir.
MsXLabs & Morpa Genel Kültür Ansiklopedisi
Son düzenleyen Safi; 25 Mayıs 2016 02:59

 Amino Asit Nedir?
Amino Asit Nedir?