ISI ve SICAKLIK
Kâinattaki tüm olaylarda ısı ve sıcaklık kavramlarının olmadığı hiçbir olay yok gibidir. Isı ve sıcaklık, canlılar için de çok önemlidir. Çünkü, çok düşük sıcaklıklarda canlılar yaşayamadığı gibi,çok yüksek sıcaklıklarda da canlılar yaşayamamaktadır.Isı enerjisi aslında kütlesi olmayan foton dediğimiz enerji paketçikleridir. Bundan dolayı ısı enerjisi boşlukta da yayılır. Bu enerji paketçikleri madde, atom ve moleküllerinin titreşim hareketinden meydana gelmektedir.
Teorik araştırmalara göre , -273 C de tüm maddelerin atom ve moleküllerinin titreşimi hemen hemen sıfır olmaktadır. Fakat şu ana kadar bu sıcaklığa inilememiştir. Isı enerjisi aynı zamanda kimyasal ve nükleer tepkimelerinde de açığa çıkmaktadır.
Isı
Bir maddenin katı, sıvı ve gaz halinde olduğu bilinmektedir. Madde bu üç halden hangisinde olursa olsun, molekülleri daima hareket halindedir. Her bir molekülün bir hareket enerjisi vardır. Bir maddenin moleküllerinin hareket enerjileri ile moleküller arası bağlanma enerjilerinin toplamına ısı enerjisi denir. Dolayısıyla ısı, madde miktarı ile doğru orantılıdır.
Sıcaklık
Bir maddenin belli bir standarda göre soğukluğunu veya ılıklığını gösteren nicelik sıcaklık olarak bilinir. Maddeyi oluşturan taneciklerin tek tek kinetik enerjileri aynı olabildiği gibi, farklı da olabilir. Bütün moleküllerin kinetik enerjileri toplanıp tanecik sayısına bölünürse ortalama bir değer bulunur. İşte sıcaklık dediğimiz şey madde moleküllerinin ortalama kinetik enerjileriyle orantılı bir büyüklüktür.
Buna göre; - Isı bir enerji çeşididir. Sıcaklık bir ölçümdür.
- Isı kalorimetre ile ölçülür. Sıcaklık termometre ile ölçülür.
- Isı birimi kalori veya joule dür. Sıcaklık birimi ise derecedir.
Isı Enerjisi
Sıcaklık, maddenin moleküllerinin hareket enerjisini ifade eden büyüklüktür. Sıcaklığı artırmak için cisme dışardan enerji vermek gerekir. Cismin sıcaklığını artırmak için verilmesi gereken enerji çeşidine ısı enerjisi denir. Q ile gösterilir.
1 kalori: 1 gram suyun sıcaklığını 1 C değiştirmek için verilmesi ya da alınması gereken ısı miktarına denir.
1 cal = 4,18 joule
Isı alıp veren maddelerde şu değişiklikler olur :
- Sıcaklık değişimi
- Hal değişimi
- Boyut değişimi
SICAKLIK DEĞİŞİMİ
Sıcaklık değişimi sırasında maddenin aldığı ya da verdiği ısı şunlara bağlıdır:
1. Maddenin alacağı ısı cismin kütlesiyle doğru orantılıdır.
2. Maddenin alacağı ısı sıcaklık artışı ya da azalışı ile doğru orantılıdır.
3. Maddenin alacağı enerjisi maddenin türüne de bağlıdır.
Öz ısı: Bir cismin birim kütlesinin sıcaklığını 1 C değiştirmek için gerekli ısı miktarına öz ısı denir. Öz ısı maddeler için ayırt edici bir özelliktir.
NOT: Bir cismin m gramının sıcaklığını At kadar artırmak için verilmesi gereken ısı miktarı
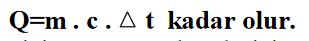 Q:
Q: Cismin sıcaklığını artırmak için veya azaltmak için verilmesi gereken ısı miktarıdır.
M: Isınan ya da soğuyan cismin gram cinsinden kütlesi C: Cismin öz ısısı
A t: Maddenin sıcaklığındaki değişme miktarıdır.
NOT: Öz ısısı küçük olan maddeler kolay ısınır. Öz ısısı büyük olan maddeler zor ısınır.
Isı Sığası (m . c): Bir maddenin kütlesi ile öz ısısının çarpımına denir.
Isı Alışverişi
Isıca yalıtılmış bir ortamda sıcaklığı yüksek olan madde sıcaklığı düşük olan maddeye ısı verir. Bu ısı aktarılması sonucunda alınan ısı verilen ısıya eşit olur.
Qal = Qver
Alınan ısı verilen ısıya eşit olmasına rağmen ısı sığaları farklı ise sıcaklık değişimleri eşit olmaz. Isı sığaları eşit ise sıcaklık değişimleri de eşit olur. Fakat son sıcaklıkları daima eşit olur.
Not: Sıcaklıkları ti ve t2 olan aynı maddeden eşit kütlede karıştırılırsa karışımın son sıcaklığı:
ÖRNEK: Farklı sıcaklıktaki X ve Y katı cisimleri birbirlerine değecek biçimde yerleştiriliyor. Cisimler arasında ısı dengesinin kurulması sürecinde X cisminin hangi nicelikleri Y nin kine kesinlikle eşit olur?
ÇÖZÜM: Farklı sıcaklıktaki cisimler birbirlerine değecek biçimde yerleştirildiğinde ve yeteri süre beklenildiğinde son sıcaklıkları eşit olur. Sıcaklık dengesinin kurulması sırasında alınan ve verilen ısı enerjileri kesinlikle eşit olur.
HAL DEĞİŞİMİ
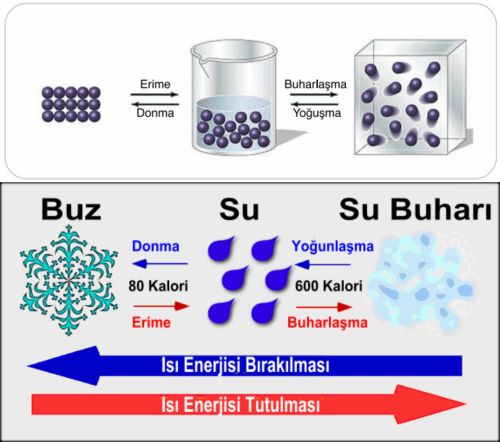
Katilar ısıtılınca molekülleri hızlanır, aralarındaki bağlar gevşer ve sıvılaşır. Sıvı molekülleri arasındaki bağlar ise koparak serbest hale gelir yani gaz haline geçer. Bu olayların tersi de meydana gelir.Gaz halindeki bir maddeden ısı alınırsa molekülleri birbirine bağlanmaya başlar ve dolayısıyla sıvılaşmaya geçerler. Sıvı halindeki bir maddeden de yeteri kadar ısı alınırsa molekülleri arasındaki mesafe azalır ve bağ kuvvetlenir. Bu olaylara hal değişimi denir. Hal değişimi olaylarında kinetik enerji değişmemekle beraber potansiyel enerji değişir.
Erime Ve Donma Olayı
Katı haldeki bir maddeye ısı verildiğinde sıcaklığı artar. Sıcaklığındaki artış miktarı,
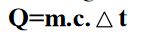
bağıntısı ile bulunur.
Cisme ısı vermeye devam edildiğinde sıcaklık öyle bir noktaya gelir ki ısı verilmesine rağmen sıcaklığı değişmez. Bunun nedeni şöyle açıklanabilir:
Isıtılan katıların molekülleri önce hızlanır. Yani kinetik enerjileri artar. Bu ise sıcaklığın artışı demektir. Isı vermeye devam ettiğimizde moleküllerin hızı öyle yükselir ki birbirlerinden uzaklaşmaya başlar. Yani erime olayı olur ve moleküller artık hızlanmazlar. Aldıkları enerjiyi birbirinden uzaklaşmak için kullanır. Dolayısıyla hal değiştirme sırasında sıcaklık sabit kalır.
Erime ve Donma Isıları
Moleküller arasındaki bağ bazı maddelerde zayıftır. Dolayısıyla bazı maddelerin moleküllerini birbirinden uzaklaştırmak için daha çok enerji, bazılarında da daha az enerji harcanır. O halde maddenin erimesi sırasında aldığı enerji maddenin cinsine ve kütlesine bağlıdır. Alınan ya da verilen ısı,
Q = m . L ifadesinden bulunur.
Burada L maddenin cinsine bağlı büyüklük olup adına ‘hal değiştirme ısısı’ denir.
Erime Isısı: Erime sıcaklığına gelmiş bir katının 1 gramının sıvı hale gelmesi için gerekli ısıya denir.
Donma Isısı: Donma sıcaklığına gelmiş bir sıvının 1 gramının donması için dışarıya vermesi gereken ısıya denir.
Erime sıcaklığı = Donma sıcaklığı
Erime ısısı = Donma ısısı
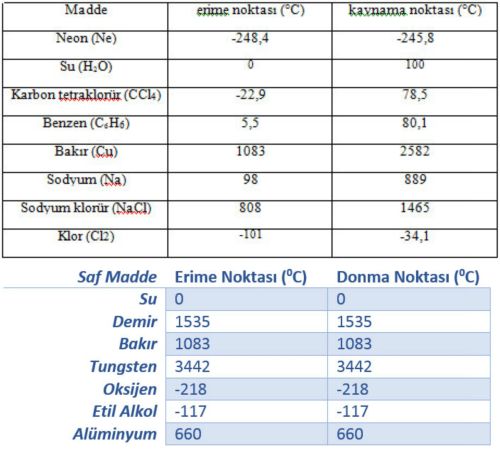
Erime ve Donma Sıcaklığına Etki Eden Faktörler
Erime ve donma noktasına iki faktör etki eder. Yani iki değişiklik yaparak erime ve donma noktaları değiştirilebilir.
Basıncın Erime ve Donmaya Etkisi
Basınç, birim yüzeye etkiyen dik kuvvettir. Bundan dolayı basınç bir maddenin moleküllerini bir arada tutarak parçalanıp dağılmasını önleyecek yönde etkir.
- Erime sırasında hacmi artan maddelerde basıncın artması erimeyi zorlaştırır. Maddenin erime sıcaklığı basınçla yükselmiş olur.
- Erime sırasında hacmi azalan maddelerde basıncın artması erimeyi kolaylaştırılır. Maddenin erime sıcaklığı düşer.
Safsızlığın Erime ve Donmaya Etkisi
Yabancı maddeler erimeye ve donmaya basınç gibi etki eder. Buzun içine tuz karıştırılması erime sıcaklığını düşürür. Suyun içine antifriz karıştırılması suyun donma sıcaklığını düşürür.
Kaynama ve Yoğunlaşma Olayları
Maddenin tamamı eridikten sonra cisme ısı vermeye devam ettiğimizde sıvının sıcaklığı artar ve bu sıcaklık artışı
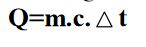
bağıntısından hesap edilir. Bu sıcaklık öyle bir noktaya gelir ki, ısı verilmesine rağmen sıcaklığında değişme meydana gelmez. Burada verilen enerji erimede olduğu gibi sıvı molekülleri arasındaki bağı koparmaya ve molekülleri birbirinden uzaklaştırmaya harcanır.
Bir maddenin ısı alarak gaz haline geçmesi olayına buharlaşma, ısı vererek gaz halinden sıvı hale geçmesi olayına da yoğunlaşma denir.
Kaynama noktası: Bir sıvının buhar basıncının atmosfer basıncına eşit olduğu andaki sıcaklığa kaynama sıcaklığı denir. 76 cm-Hg basıncında saf suyun kaynama sıcaklığı 100 C dir.
Yoğunlaşma sıcaklığı: Yoğunlaşma olayı kaynama olayının tersinir durumudur. Sabit basınç altında gaz haldeki madde yoğunlaşarak sıvı
hale geçerken sıcaklığı değişmez. Bu sıcaklık değerine yoğunlaşma sıcaklığı denir.
Bu durumda kaynama ve yoğunlaşma noktaları aynı olur. Kaynama ve yoğunlaşma noktaları madde miktarına bağlı değildir.
Yoğunlaşma ısısı: Yoğunlaşma sıcaklığına gelmiş 1 gram buharın 1 gram sıvı haline gelmesi için dışarıya vermesi gerekli ısıya o buharın yoğunlaşma ısısı denir.
Bir maddenin ;
Kaynama sıcaklığı = Yoğunlaşma sıcaklığı
Kaynama ısısı = Yoğunlaşma ısısıdır.
Erime ve buharlaşma olaylarının tersi donma ve yoğunlaşmadır. Sabit bir basınçta erime ve kaynama sıcaklığı, erime ve kaynama ısısı maddeler için ayırt edici bir özelliktir.
Kaynama ve Yoğunlaşma Sıcaklıklarına Etki Eden Faktörler
Basıncın Kaynamaya Etkisi - Kaynama olayının gerçekleşmesi için sıvının buhar basıncının atmosfer basıncına eşit olması gerekir. Buna göre atmosfer basıncı artarsa kaynama zorlaşır. Yani kaynama noktası yükselir. Düdüklü tencerede buhar basıncının artması kaynama noktasını 110 C veya 120 C’ lere yükseltir. Dolayısıyla yemek daha iyi pişer.
- Basınç azalırsa kaynama noktası düşer. Deniz seviyesinden yükseldikçe açık hava basıncı azalacağından kaynama noktası düşer. Erzurum’da saf su yaklaşık 94 C de kaynar. Everest dağının tepesinde 75 C de kaynar.
- Eğer yeryüzünde atmosfer olmasaydı bütün sular kaynayarak uzaya yayılırdı.
Buharlaşma
Sıvıların gaz haline geçmesi olayına buharlaşma denir. Buharlaşmada basınç ve diğer fiziksel şartların etkisi çoktur. Sıvı ısıtıldığında moleküllerin hızı artar. Hızla sıvı yüzeyine ulaşan molekül, moleküller arası çekim kuvvetini ve yüzey gerilimini yenerek sıvıyı terk eder. Bu olaya
buharlaşma denir.
Buharlaşma Isısı: Kaynama sıcaklığındaki 1 gram sıvının buharlaşarak, aynı sıcaklıkta 1 gram buhar haline gelmesi için gerekli ısıya o sıvının buharlaşma ısısı denir.
- Buharlaşma her sıcaklıkta olabilir.
- Buharlaşma ısı soğurmayı gerektirir.Bütün soğutma makinelerinde özel bir sıvı buharlaştırılarak soğuma sağlanır. Testinin içindeki suyun soğuması buharlaşmanın bir sonucudur.
- Basıncın artması buharlaşmayı zorlaştırır.Azalması ise buharlaşmayı kolaylaştırır. Rüzgarlı havalarda çamaşırların kolay kurumasının sebebi akışkanın hızının arttığı yerde basıncın azalmasındandır.
- Sıvının açık yüzeyinin artması buharlaşmayı arttırır.
- Buharlaşma hızı sıcaklıkla doğru orantılıdır.
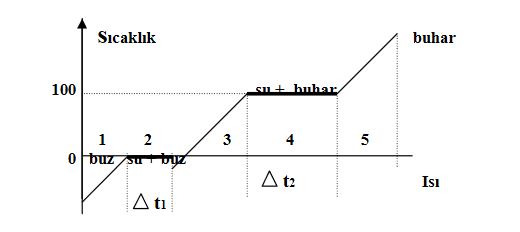
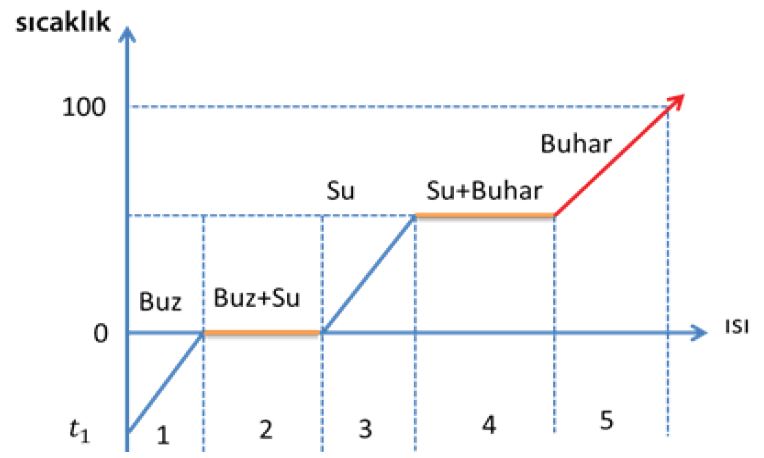
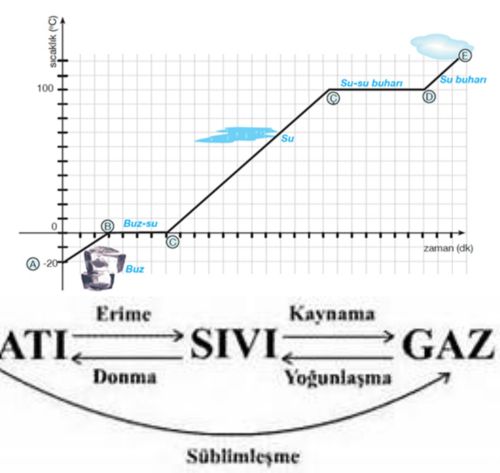
Bir miktar buz parçasına verilen ısının sıcaklığa göre değişim grafiği şekildeki gibidir. Grafikte sıcaklığın değişmediği yerlerde madde hal değiştirmektedir. Yani hal değiştirme sırasında sıcaklık atışı gözlenmez.
Bir miktar buzu katı halden buhar haline getirmek için verilmesi gereken ısı grafiğin 1,2,3,4,5 aralıklarında ayrı ayrı verilmesi gereken ısıların toplamına eşittir.
- Buzun erime ısısı Le: 80 cal/g, suyun kaynama ısısı Lk=540 cal/g olduğundan, ısı hızı sabit ocakla ısıtıldığında, grafikte ti süresi t2 süresinden daha küçüktür.
- Grafikteki doğruların eğimi, t/Q =1/m . c dir.
Önemli Uyarılar
1. Isı alan veya veren bir madde hem hal değişikliği hem de sıcaklık değişiminin ikisini de yapabilir.
2. Sıcaklığı değişen bir maddenin kinetik enerjisi, hal değişikliği yapan bir maddenin de potansiyel enerjisi değişir.
3. Hal değişikliği yapan maddelerde erime ve kaynama süreleri madde miktarına bağlıdır.
4. Birden fazla sıvı karışımın olduğu bir kabı ısıttığımızda ilk önce kaynama noktası en küçük olan sıvı buharlaşır. Diğer sıvılarda bu sırayı takip eder. Kaptaki sıvının birisi kaynarken karışımdaki diğer sıvıların sıcaklığı değişmez.
5. Sıcaklıkları eşit olan maddelerde ısı alış-verişi olmaz.
6. Bir maddenin katı halden sıvı hale geçerken ve sıvı halden gaz hale geçerken yoğunluğu değişir.
7. Su hariç maddelerin yoğunlukları sıcaklıkla ters orantılıdır.
BOYUT DEĞİŞİMİ (GENLEŞME)
Genleşmeler ve Büzülmeler
Isı alan cisimlerin hareketleri hızlanır ve molekülleri arasındaki uzaklık artar. Bunun sonucunda da cisim genleşir yani hacmi artar. (Buz hariçtir. Buzun özel durumu vardır)
Bütün genleşmeler aslında hacimcedir. Uzun bir demir çubuk ısıtıldığı zaman boyu uzar, boyu uzamanın yanında kalınlığı da artar. Ancak kalınlığındaki artış boyundaki uzamanın yanında ihmal edilecek kadar küçük olduğundan bu olay sadece boyca uzama diye adlanır. Keza bunun gibi bir metal levha ısıtıldığında metal levhanın yüzeyi artar, yüzeyin artmasıyla birlikte kalınlığı da artar. Ancak kalınlığındaki artış yüzeyindeki artışın yanında ihmal edilecek kadar küçük olduğu için bu olay sadece yüzeyce genleşme diye adlandırılır.
Netice olarak diyebiliriz ki ısıtılan cisimlerin hacimlerinde meydana artışa genleşme denir. Bu olayın tersi ise büzülmedir. Üzerinden ısı alınan cisimlerin hacimlerinde meydana gelen küçülmeye büzülme denir.
Genleşme Nelere Bağlıdır?
Maddelerin ilk hacimleri büyükse aynı sıcaklık değişiminde genleşme miktarı da artar. O halde genleşme miktarı maddenin ilk hacmi ile doğru orantılıdır.
Faklı metallerin molekülleri arasındaki boşluk da farklıdır. Örneğin bakırın molekülleri arasındaki boşluk ile kurşunun molekülleri arasındaki boşluk aynı değildir. Bu nedenle genleşmeleri de aynı değildir. O halde genleşme, maddenin cinsine bağlıdır.
Sıcaklık artışı ne kadar çok olursa maddenin molekülleri de o kadar çok hızlanır. Bundan da anlaşılacağı gibi genleşme, sıcaklık artışı ile doğru orantılıdır.
Netice olarak ısıtılan bir maddenin, ilk hacmi V0, sıcaklığındaki artma t ise hacmindeki artma miktarı
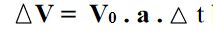
bağıntısından bulunur.
Katilarda Genleşme Olayı
Isıtılan metal üç boyutta da uzadığından, boyca, yüzeyce, hacimce genleşmiş olur.
Boyca Uzama
 Önemli Uyarılar
Önemli Uyarılar
1. Boyca genleşme kat sayısı sadece katının cinsine bağlıdır. Katılar için ayırt edici özelliktir.
2. Aynı cins maddeden yapılan iki metalin ilk boyları aynı, kalınlıkları farklı olsun. Sıcaklık değişimleri aynı olacak şekilde ısıtıldığında son boyları yine aynı olur.
3. Aynı cins maddeden yapılan iki metalin ilk boyları aynı kütleleri farklı olsun. İlk sıcaklıları aynı olan bu metallere eşit miktarda ısı verdiğimizde son boyları eşit olmaz. Çünkü kütlesi büyük olanın sıcaklık artışı daha az olacağından uzama miktarı da az olur.
4. Aynı cins maddeden yapılan iki metalin ilk boyları ve sıcaklıkları aynı olsun. Sıcaklık farkları aynı olacak şekilde birisini ısıtıp diğerini soğuttuğumuzda , ısıtılanın boyu artar , soğutulanın boyu azalır. Ancak uzama ve kısalma miktarları aynı olur.
5. Birbirine perçinlenmiş X ve Y metal çubukları ısıtıldığında ve soğutulduğunda birbirlerini bırakmadıkları için bükülürler. Uzama kat sayısı büyük olan ısıtıldığında daha fazla uzar, soğutulduğunda daha fazla büzülür.
Yüzeyce Genleşme
 Önemli Uyarı
Önemli Uyarı
1. Aynı cins maddeden yapılan iki metalin ilk yüzeyleri ve sıcaklıkları aynı, kalınlıkları farklı olsun. Kalınlıkları farklı olunca kütleleri de farklı olur. Bu metallere eşit miktarda ısı verelim. Kalın levhanın kütlesi ince levhanın kütlesinden büyük olduğu için, Q= m. c. At ye göre kütlesi büyük olanın sıcaklık değişimi küçük olur. Böylece yüzeyce genleşmeleri de farklı olur.
Hacimce Genleşme
 Önemli Uyarılar
Önemli Uyarılar
1. Aynı cins maddeden yapılan iki metal küreden birisinin boş, diğerinin içi dolu olup dış hacimleri ve ilk sıcaklıkları eşit olsun. Bu metal küreleri sıcaklık değişimleri eşit kalmak şartıyla ısıttığımızda ve soğuttuğumuzda dış hacimleri yine eşit olur.
2. Aynı şartlardaki metal kürelere eşit miktarda ısı verelim. İçi boş kürenin kütlesi, içi dolu olan kürenin kütlesinden küçük olduğu için,
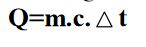
ye göre Kütlesi küçük olanın sıcaklık değişimi büyük olur. Sonuçta eşit ısı verilen içi boş kürenin son hacmi daha büyük olur.
3. Sıvılar için hacimce genleşme kat sayısı ( a) verilir.
Sıvılarda Genleşme Olayı
Sıvılar kaba doldurulduklarında kabın şeklini aldıklarından bir geometrik şekli yoktur. Dolayısıyla boyca ve yüzeyce genleşmeden bahsetmek oldukça güçtür. Hacimsel olarak genleşmelerini incelemek ise oldukça kolaydır. Sıvının hacimsel olarak genleşme miktarı ,
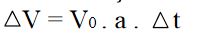
bağıntısından bulunur.
Burada;
V0: Sıvının t sıcaklığındaki hacmi
A: Hacimsel olarak genleşme katsayısıdır.
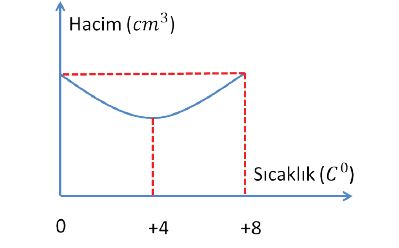
Su ise farklı özellik gösterir. Suyun 1 atmosferlik basınç altında +4 C altında ve üstündeki sıcaklıklarda suyun hacmi artar. Eğer suyun diğer sıvılardan farklı özelliği olmasaydı yani diğer sıvılar gibi davransaydı, sular üstten değil dipten donardı. Dolayısıyla denizlerde hayat olmazdı. Hâlbuki su üstten donup 1 m kalınlığında buz tabakası olsa da, suyun dip taraftaki sıcaklığı +4 civarındadır. Çünkü yoğunluğu en fazla olan sıvı dipte olur. Bizmut ve Antimon da su gibi davranır.
Gazlarda Genleşme Olayı
Gazlarda genleşme olayı sabit basınç altında olur. Kapalı kaplardaki gazların genleşmelerinden bahsedilemez. Genleşme katsayısı bütün gazlar için aynıdır. Dolayısıyla genleşme kat sayısı gazlar için ayırt edici bir özellik değildir.
 Örnek:
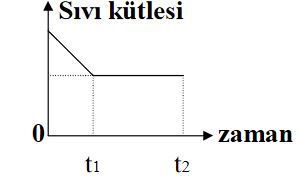
Örnek: Bir kaptaki sıvı eşit zaman aralıklarında eşit enerji veren bir ısıtıcı ile 0—12 zaman aralığında ısıtılıyor. Bu arada kaptaki sıvı kütlesi-zaman grafiği gibidir.
Grafiğin yorumunu yapınız?
Çözüm:
Sıvıya 0-tı zaman aralığında sürekli ısı verildiği halde, sıvının kütlesi önce azalıyor sonra sabit kalıyor. Demek ki sıvı bir karışımdır ve karışımdaki kaynama noktası düşük olan sıvı gaz haline geçip kaptan ayrılıyor.
Sıvılardan biri hal değiştirirken kapta kalan diğer sıvının sıcaklığı sabit kalır. tı-t2 zaman aralığında ise kapta kaynama noktası yüksek olan diğer sıvı bulunmaktadır. Bu aralıkta kütle kaybolmadığına göre cisim hal değiştirmiyordur. Fakat ısı aldığından dolayı sıcaklığı artıyor ve genleşmesi sonucu öz kütlesi azalıyor.
Isı İletimi ve Yalıtımı
Sıcak ve soğuk maddeleri muhafaza eden termoslar, evlerin sıcak ve soğuktan korunması için ısı yalıtımını yapılması pencerelerin çift cam yapılması, kuşların tüylerini kabarması, su borularının izocamla sarılması gibi olaylar ısının yalıtımı ile ilgilidir. Isı aktarımı üç değişik yolla olmaktadır.
1. İletim yoluyla
2. Konveksiyon yoluyla
3. Işıma yoluyla
İletim
Isının bu yolla yayılması katılarda olur. Isıyı alan katı taneciklerinin hareket enerjileri artar. Bu tanecikler yerlerinden ayrılmayacağından titreşimleri artacak demektir. Titreşirken çevrelerindeki diğer tanecikleri de titreşime zorlarlar. Yani hareket enerjilerini çevrelerine de verirler. Böylece enerji tanecikte taneciğe iletilmiş olur.
Katı maddeler ısıyı bu şekilde iletirken bazı maddeler hızlı, bazı maddeler yavaş iletirler. Yani katıların ısı iletkenlikleri farklı farklıdır.
Mesela ocaktaki çorbayı metal kaşıkla karıştırırsak elimizin çabuk yandığını, tahta kaşıkla karıştırırsak elimizin yanmadığını görürüz. Bunun nedeni metalin ısıyı daha çabuk iletmesidir.
Örnek: Serin bir günde parkta tahta sırada oturmakta olan bir adam, beton bir sıraya geçerse daha fazla üşümeye başlar. Bunun nedeni nedir?
Çözüm: Adamın betonda daha fazla üşümesinin sebebi ısı iletkenliğidir. Beton ısıyı tahtadan daha iyi iletir. Beton ısıyı adamdan çeker. Dolayısıyla adam üşür. Betonun sıcaklığı tahtanın sıcaklığına eşittir. Çünkü ikisi de aynı ortamda olduğu için sıcaklık dengesi kurulmuştur. Dolayısıyla beton sırada oturanın üşümesi betonun sıcaklığının düşük olmasından değildir.
Konveksiyon
Sıvı ve gazlar kolay hareket edebilen akışkan maddelerdir. Isınan maddelerin hacmi artar dolayısıyla da yoğunluğu azalır. Yoğunluğu azalan sıvı ve gaz molekülleri yukarı doğru hareket ederler.
Isı kaynağından enerjiyi alan tanecikler başka yerlere giderken ısıyı da beraberinde taşırlar. Buna en iyi örnek soba ve kaloriferli odalardır. Sobada veya kalorifer peteğinde ısınan hava tanecikleri ısıyı beraberinde taşıyarak odayı ısıtır. Moleküllerin hareketinde dolayı oda içinde hafif rüzgârcıklar oluşur. Isını bu yolla yayılması sadece sıvı ve gazlarla mümkündür.
Örnek: Yeterince uzun 0 C de su dolu tüpün dibine yukarı çıkmayacak şekilde buz parçaları konuluyor. Suyun üst tarafı iyice ısıtılmasına rağmen buz erimiyor.
Bunun nedeni nedir?
Çözüm: Su alttan ısıtıldığında genleşen suyun öz kütlesi azalarak yukarı çıkar. Yukarıdaki soğuk ve öz kütlesi büyük olan su aşağı inerek konveksiyon akımı oluşturur. Su üstten ısıtıldığında öz kütlesi küçük olan ısınmış su aşağı inemez ve aşağıdaki soğuk su yukarı çıkamaz. Yani konveksiyon akım oluşmaz. Su kötü iletken olduğu için iletim yoluyla da ısı iletilemez. Böylece buz erimez.
Işıma
Kaynaktan çıkan ısı enerjisinin etrafa doğru enerji şeklinde yayılmasıyla gerçekleşir. Isı ışık gibi davranır. Yani boşlukta da yayılır. Parlak yüzeyler tarafından yansıtılır, mat yüzeyler tarafından soğurulur. Dolayısıyla ısıyı soğuran madde ısınır. Isının dünyamıza gelmesi bu yolla olur.
Isının iletim ve konveksiyon yoluyla yayılması için bir madde gerektiği halde ışıma yoluyla yayılması için bir maddeye ihtiyaç yoktur.
Bütün cisimler çevrelerine az veya çok ışıma yoluyla ısı verirler. Bu ısı verme cismin sıcaklığına ve yüzeyinin yapısına bağlıdır.
kaynak: S.Gülçek
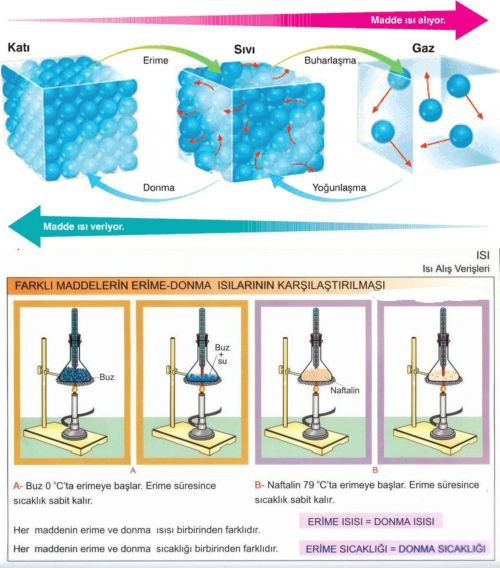
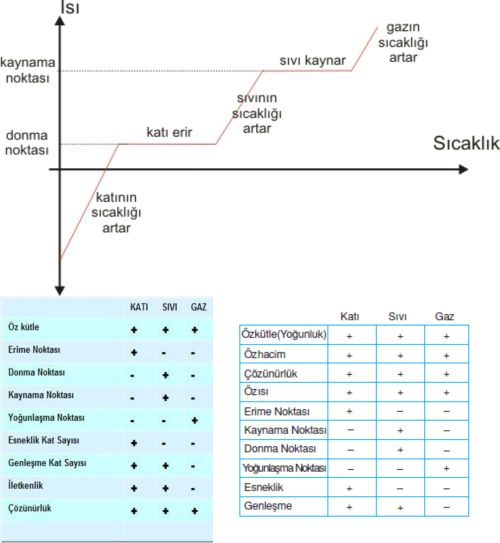

 Maddenin Hal Değişimi
Maddenin Hal Değişimi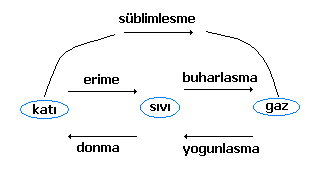
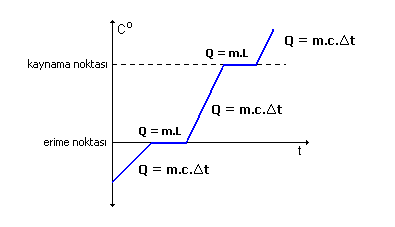
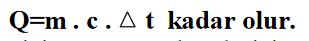
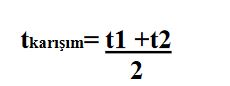
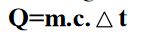 bağıntısı ile bulunur.
bağıntısı ile bulunur.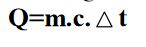 bağıntısından hesap edilir. Bu sıcaklık öyle bir noktaya gelir ki, ısı verilmesine rağmen sıcaklığında değişme meydana gelmez. Burada verilen enerji erimede olduğu gibi sıvı molekülleri arasındaki bağı koparmaya ve molekülleri birbirinden uzaklaştırmaya harcanır.
bağıntısından hesap edilir. Bu sıcaklık öyle bir noktaya gelir ki, ısı verilmesine rağmen sıcaklığında değişme meydana gelmez. Burada verilen enerji erimede olduğu gibi sıvı molekülleri arasındaki bağı koparmaya ve molekülleri birbirinden uzaklaştırmaya harcanır.
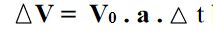 bağıntısından bulunur.
bağıntısından bulunur.



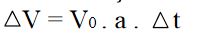 bağıntısından bulunur.
bağıntısından bulunur.
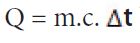 bağıntısı ile bulunur.
bağıntısı ile bulunur.